回顧2022,盡管資本寒冬席卷創新藥領域,但(dàn)是新技(jì)術(shù)、新療法的發展并未停下腳步,細胞療法領域依然蓬勃發展。其中,CAR-T療法多(duō)樣化明(míng)顯出現,新靶點和(hé)适應症陸續獲批,改善CAR-T療效的各種新技(jì)術(shù)也層出不窮。此外,行(xíng)業對NK細胞這種通(tōng)用現貨型藥物平台也充滿期待,新成立的細胞藥物研發公司大(dà)多(duō)數(shù)選擇NK細胞作(zuò)為(wèi)平台技(jì)術(shù),進軍CAR-NK領域。展望2023,醫(yī)藥魔方綜合過去一年細胞療法領域交易合作(zuò)/投融資、重大(dà)進展、技(jì)術(shù)特色等,篩選了10家(jiā)值得(de)關注的細胞療法公司,以供參考。
核心技(jì)術(shù):下一代自體(tǐ)和(hé)同種異體(tǐ)CAR-T
2022動向:與羅氏達成超60億美元的合作(zuò)+ 增發8050萬美元
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://poseida.com/
Poseida Therapeutics是一家(jiā)總部位于美國聖地亞哥(gē)的臨床階段生(shēng)物制(zhì)藥公司,緻力于利用專有(yǒu)的基因工程平台技(jì)術(shù)來(lái)創造具有(yǒu)治愈能力的下一代細胞和(hé)基因療法,并且由自體(tǐ)逐漸轉向同種異體(tǐ)CAR-T療法。
該公司的CAR-T細胞不含有(yǒu)單鏈可(kě)變片段(scFv)結構,而是由全人(rén)源的Centyrin結構域組成。Centyrin是一種小(xiǎo)型、簡單、高(gāo)度穩定的蛋白質,能以很(hěn)高(gāo)的特異性和(hé)親和(hé)力結合目标抗原,在穩定性高(gāo)的同時(shí)具有(yǒu)低(dī)免疫原性。
不同于傳統的病毒載體(tǐ)系統,Poseida專有(yǒu)的piggyBac DNA修飾系統使用非病毒載體(tǐ)将CAR分子基因遞送給T細胞,可(kě)以産生(shēng)具有(yǒu)高(gāo)百分比T記憶幹細胞(TSCM細胞)的CAR-T産物。TSCM細胞具有(yǒu)自我更新能力和(hé)多(duō)能性,高(gāo)TSCM細胞占比可(kě)以使候選藥物更有(yǒu)效、毒性更小(xiǎo)、更耐用;非病毒載體(tǐ)制(zhì)造成本低(dī)、生(shēng)産時(shí)間(jiān)短(duǎn)、誘變和(hé)腫瘤發生(shēng)的風險低(dī);同時(shí),PiggyBac的載貨量可(kě)達慢病毒載體(tǐ)的20倍,可(kě)以有(yǒu)效遞送超大(dà)片段基因,實現穩定的轉基因表達。
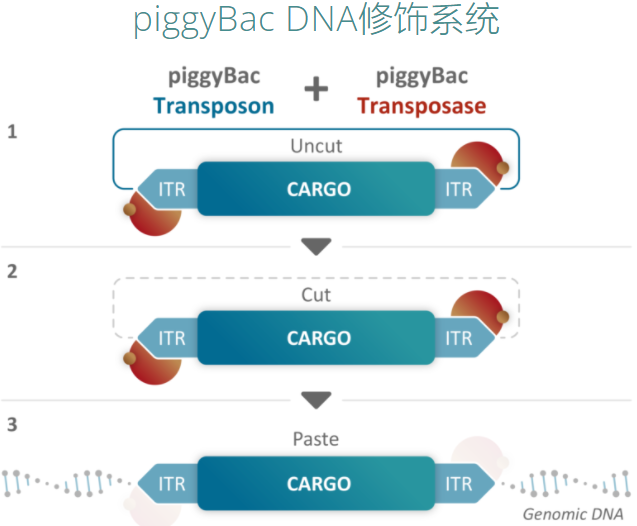 來(lái)源:Poseida官網
來(lái)源:Poseida官網
此外,Poseida使用Cas-CLOVER系統敲除CAR-T細胞中多(duō)種T細胞關鍵抑制(zhì)信号的受體(tǐ),可(kě)以保證CAR-T細胞的活化狀态。Cas-CLOVER使用了一種被稱為(wèi)dCas9的Cas9酶,這種酶無法切割DNA,隻有(yǒu)在與适當的引導RNA結合時(shí)才起到DNA 結合蛋白的作(zuò)用。該系統能有(yǒu)效的避免TALEN技(jì)術(shù)隻能用于激活的細胞的使用限制(zhì)性和(hé)CRISPR/Cas9可(kě)能的脫靶突變帶來(lái)的潛在安全風險。
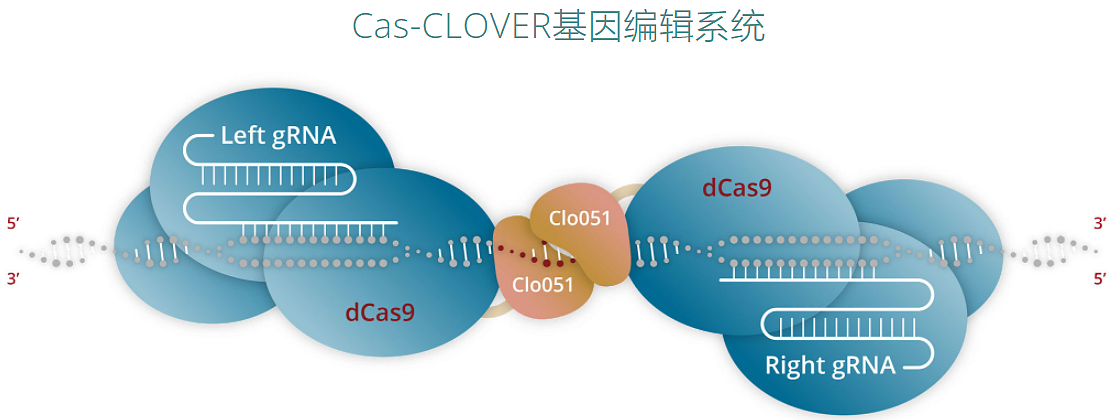 來(lái)源:Poseida官網
來(lái)源:Poseida官網
綜合來(lái)看,Poseida的在研産品旨在解決其他CAR-T療法的局限性,包括反應持續時(shí)間(jiān)、治療實體(tǐ)腫瘤的能力和(hé)安全性問題,其轉染、編輯以及遞送平台都有(yǒu)獨特優勢,可(kě)能帶來(lái)成本更低(dī)、生(shēng)産時(shí)間(jiān)更短(duǎn)的CAR-T療法,解決當下的瓶頸。
該公司的技(jì)術(shù)平台也得(de)到了大(dà)藥企的認可(kě):2021年10月,與武田就新型非病毒體(tǐ)內(nèi)基因療法開(kāi)展高(gāo)達36億美元的研究合作(zuò);2022年8月,Poseida宣布與羅氏達成總額超60億美元的全球戰略合作(zuò)與許可(kě)協議,這也是2022年細胞療法領域金額最高(gāo)的“License in”交易。羅氏将從Poseida獲得(de)獨家(jiā)授權,對Poseida産品組合中針對血液惡性腫瘤的一些(xiē)同種異體(tǐ)CAR-T項目進行(xíng)開(kāi)發和(hé)商業化。在與羅氏合作(zuò)的消息發布之後,Poseida的股價暴漲了85%。
核心技(jì)術(shù):“可(kě)控”自體(tǐ)和(hé)同種異體(tǐ)CAR-T
2022動向:與吉利德旗下Kite達成潛在總額超40億美元合作(zuò) + IPO 1.423億美元 + 增發1.288億美元
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://www.arcellx.com/
總部位于美國馬裏蘭州的Arcellx緻力于開(kāi)發更安全、更有(yǒu)效、更廣泛的創新免疫療法,以治療癌症和(hé)其它無法治愈的疾病。
2022年2月8日,公司宣布完成IPO,此次發行(xíng)的總收益為(wèi)1.423億美元。所獲資金将用于推動其主打CAR-T療法(CART-ddBCMA)進入關鍵性臨床試驗,治療複發/難治性多(duō)發性骨髓瘤(r/r MM),以及推動其“可(kě)控”CAR-T在研療法進入臨床開(kāi)發階段。CART-ddBCMA已獲FDA授予的快速通(tōng)道(dào)資格、先進再生(shēng)醫(yī)學療法認定,和(hé)孤兒藥資格。IPO前Arcellx累計(jì)融資超2億美元。
鑒于現有(yǒu)的細胞治療方案大(dà)多(duō)使用基于生(shēng)物的scFv結合域,往往隻對有(yǒu)限的部分患者有(yǒu)益,還(hái)常常導緻高(gāo)毒性,并且在可(kě)治療适應症中的适用性狹窄。Arcellx通(tōng)過設計(jì)一類新的D-Domain驅動的自體(tǐ)和(hé)同種異體(tǐ)CAR-T細胞來(lái)克服這些(xiē)限制(zhì),包括經典的單次輸注CAR-T(稱為(wèi)ddCARs)和(hé)可(kě)劑量控制(zhì)的通(tōng)用型CAR-T(稱為(wèi)ARC-SparX)。
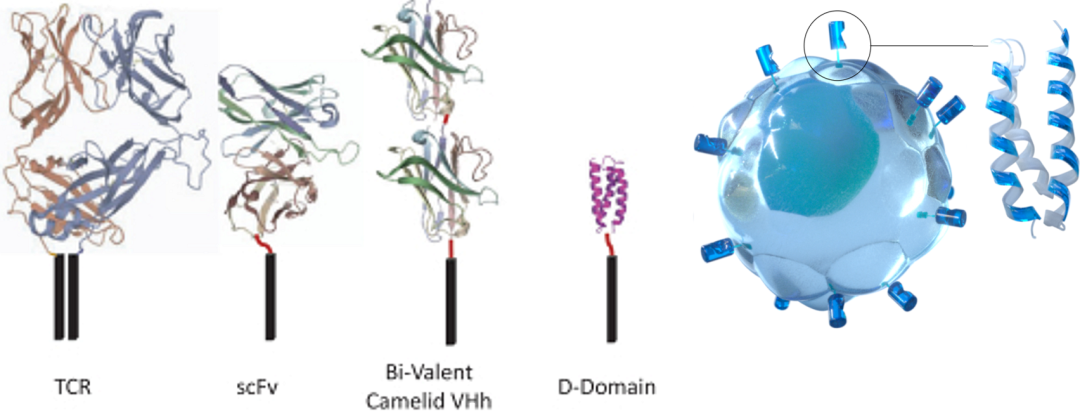 D-Domain是一種小(xiǎo)型、穩定、全合成的接合劑,具有(yǒu)疏水(shuǐ)核。當用于CAR時(shí),其獨特的結構可(kě)能實現更高(gāo)的轉導效率、更高(gāo)細胞表面表達和(hé)更低(dī)的強直信号傳導,其設計(jì)目的是提高(gāo)靶标特異性,同時(shí)增強結合親和(hé)力。D-Domain的獨特性允許生(shēng)成專有(yǒu)靶标結合域的多(duō)樣庫,并作(zuò)為(wèi)Arcellx專有(yǒu)的ddCAR和(hé)ARC-SparX平台的基礎。(來(lái)源:Arcellx招股書(shū)和(hé)官網)
D-Domain是一種小(xiǎo)型、穩定、全合成的接合劑,具有(yǒu)疏水(shuǐ)核。當用于CAR時(shí),其獨特的結構可(kě)能實現更高(gāo)的轉導效率、更高(gāo)細胞表面表達和(hé)更低(dī)的強直信号傳導,其設計(jì)目的是提高(gāo)靶标特異性,同時(shí)增強結合親和(hé)力。D-Domain的獨特性允許生(shēng)成專有(yǒu)靶标結合域的多(duō)樣庫,并作(zuò)為(wèi)Arcellx專有(yǒu)的ddCAR和(hé)ARC-SparX平台的基礎。(來(lái)源:Arcellx招股書(shū)和(hé)官網)
2022年12月9日,Arcellx公布了CART-ddBCMA在r/r MM中的I期臨床試驗數(shù)據,患者ORR達到100%,38例可(kě)評估患者中27例(71%)達到CR或sCR,34例(89%)達到非常好的部分緩解(VGPR)以上(shàng)的緩解。同一日,吉利德科學旗下Kite宣布與Arcellx達成潛在總額超40億美元的研發合作(zuò)協議,将共同開(kāi)發和(hé)商業化Arcellx的臨床後期在研療法CART-ddBCMA,用于治療r/r MM患者。
核心技(jì)術(shù):iPSC衍生(shēng)的CAR-iNK和(hé)CAR-iT細胞療法
2022動向:與百時(shí)美施貴寶達成超30億美元合作(zuò)+增發5000萬美元
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://www.centurytherapeutics.com/
Century Therapeutics成立于2018年,總部位于美國費城,是一家(jiā)面向新興的即用型同種異體(tǐ)細胞療法領域,專注于同種異體(tǐ)、誘導多(duō)能幹細胞(iPSC)衍生(shēng)的CAR-iNK和(hé)CAR-iT細胞療法的創新生(shēng)物技(jì)術(shù)公司。
2019年7月1日,Century走出隐身模式,獲得(de)了來(lái)自拜耳、Versant以及富士膠片株式會(huì)社子公司FCDI高(gāo)達2.5億美元的融資,用于推進其多(duō)項血液腫瘤和(hé)惡性實體(tǐ)瘤研究進入臨床階段。2021年3月,Century宣布完成1.6億美元的C輪融資;6月,公司在納斯達克正式上(shàng)市,拟募資2.11億美元。2022年1月,Century與百時(shí)美施貴寶(BMS)達成一項總額超30億美元的研究合作(zuò)和(hé)許可(kě)協議,以聯合開(kāi)發和(hé)商業化iPSC衍生(shēng)的同種異體(tǐ)細胞療法,計(jì)劃用于治療血液系統惡性腫瘤和(hé)實體(tǐ)瘤。
Century在iPSC衍生(shēng)療法領域的大(dà)步向前離不開(kāi)其技(jì)術(shù)平台的5個(gè)關鍵要素:
1)高(gāo)效精準的基因編輯技(jì)術(shù):提高(gāo)基因組精确性與完整性;
2)專有(yǒu)的ALLO-EVASION™技(jì)術(shù):降低(dī)患者免疫排斥,有(yǒu)望重複給藥;
3)CAR與蛋白質編輯:針對腫瘤異質性和(hé)抗原缺失問題;
4)通(tōng)用型工程化iPSC前體(tǐ):其無限自我更新能力的iPSC技(jì)術(shù)能夠降低(dī)新産品開(kāi)發的設計(jì)投入,加速候選産品研發的叠代;
5)簡化的制(zhì)造過程。
目前,公司正在整合一系列同種異體(tǐ)iNK和(hé)iT細胞治療産品候選産品,涵蓋實體(tǐ)瘤和(hé)血液系統惡性腫瘤。所有(yǒu)候選産品均采用專有(yǒu)的Allo-Evasion™技(jì)術(shù),以避免宿主排斥反應,并可(kě)能提高(gāo)臨床應答(dá)的持久性。
 Century在研管線(來(lái)源:Century官網)
Century在研管線(來(lái)源:Century官網)
其中主要候選産品CNTY-101為(wèi)iPSC來(lái)源的通(tōng)用型CAR-iNK療法,被改造表達CD19 CAR、可(kě)溶性IL-15與EGFR安全開(kāi)關。具體(tǐ)來(lái)說:1)使用Allo-Evasion™技(jì)術(shù)删除β2M以消除HLA-1的表達,防止自體(tǐ)T細胞殺傷;加入HLA-E表達,以結合NKG2A,防止自體(tǐ)NK細胞殺傷;2)納入穩态細胞因子IL-15,增加持久性和(hé)功能性;3)安全開(kāi)關可(kě)允許通(tōng)過注射西妥昔單抗的ADCC作(zuò)用抹除表達EGFR的細胞,旨在必要時(shí)在體(tǐ)內(nèi)快速清除細胞。
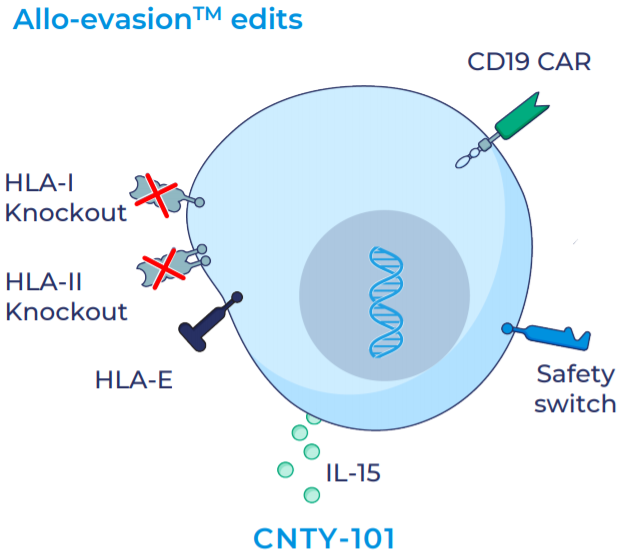 CNTY-101結構示意圖(來(lái)源:Century)
CNTY-101結構示意圖(來(lái)源:Century)
2022年8月25日, Century宣布美國FDA已批準CNTY-101的IND申請(qǐng),用于複發/難治性B細胞惡性腫瘤的治療。
核心技(jì)術(shù): CAR-γδ T細胞療法;TCR-γδ T細胞療法
2022動向:與BMS達成超14億美元合作(zuò) + 與 Editas Medicine達成未披露金額的合作(zuò)
魔方評分:⭐⭐⭐⭐
公司官網:https://immatics.com/
Immatics成立于2000年,孵化自德國Tübingen大(dà)學的H.G. Rammensee實驗室,是一家(jiā)活躍于發現和(hé)開(kāi)發T細胞重定向癌症免疫療法的生(shēng)物技(jì)術(shù)公司,專注于免疫治療藥物的發現。
基于其獨特的靶點(XPRESIDENT®平台)和(hé)T細胞受體(tǐ)(XCEPTOR®平台)發現能力,Immatics開(kāi)發了廣泛而多(duō)樣的癌症免疫治療組合,建立了包括ACTengine®(自體(tǐ))、ACTallo®(異體(tǐ))、TCER®(雙特異性)方法為(wèi)基礎的T細胞療法。
ACTengine®是一種個(gè)性化TCR-T療法,患者自身的T細胞經過基因修飾,以表達新的專有(yǒu)TCR,然後将修飾的T細胞重新注入患者體(tǐ)內(nèi),以與腫瘤特異性結合。
ACTallo®是γδT細胞衍生(shēng)的同種異體(tǐ)“現貨型”細胞療法。
TCER®是一種工程化“現貨型”生(shēng)物制(zhì)劑,旨在結合患者的循環T細胞,并将其帶到癌細胞附近并加以摧毀。其由一個(gè)直接識别癌細胞的TCR和(hé)一個(gè)招募及激活患者T細胞的T細胞招募域組成。
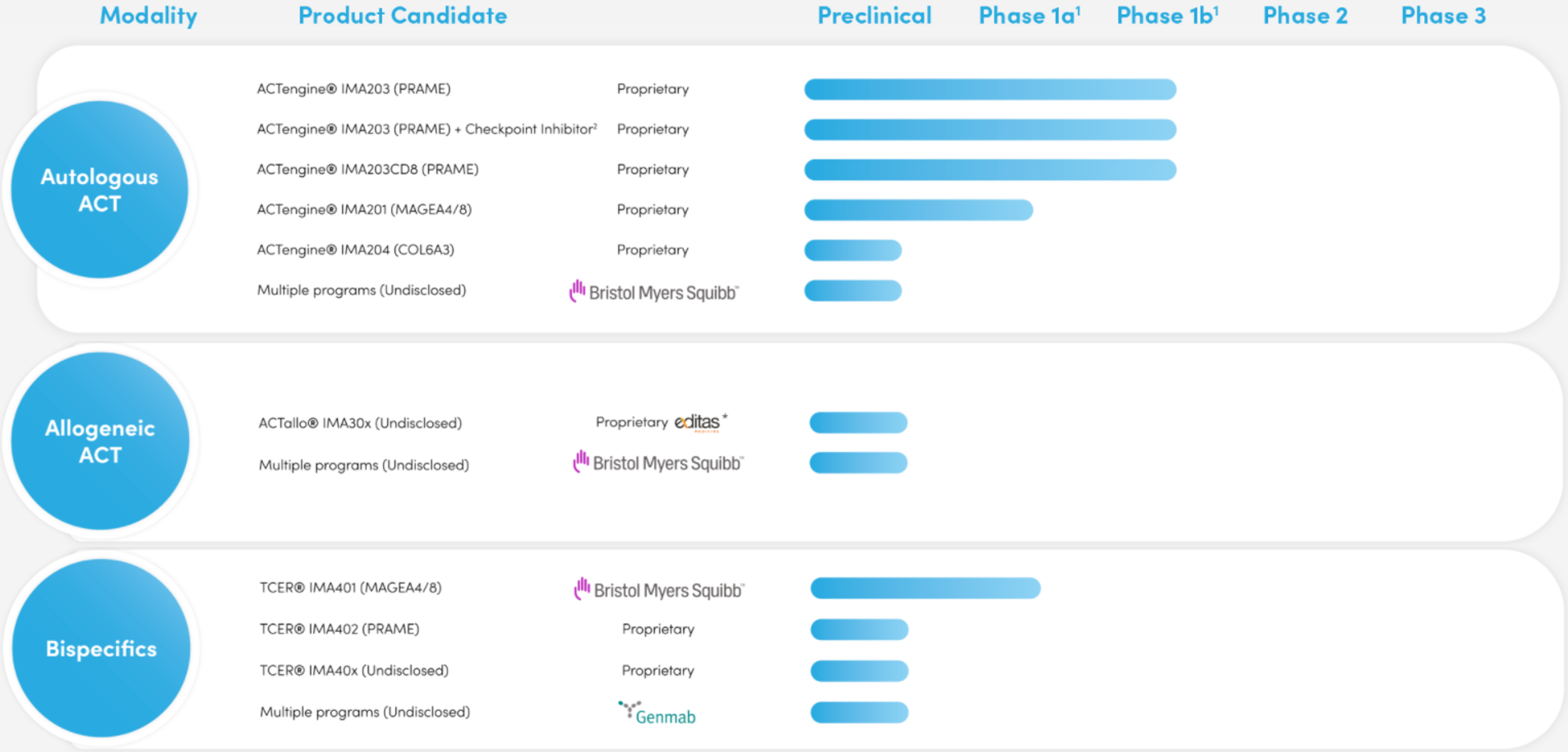 Immatic在研管線(來(lái)源:Immatic官網)
Immatic在研管線(來(lái)源:Immatic官網)
2022年10月10日,Immatics公布了其TCR-T療法ACTengine® IMA203的積極中期數(shù)據,在Ib期臨床試驗部分,接受治療的5例患者中有(yǒu)4例(80%)獲得(de)确認客觀緩解。根據初步結果,公司同時(shí)宣布了一項新的公開(kāi)募股,融資1.1億美元。
事實上(shàng),Immatics是TCR-T領域的吸金王,曾受到了各大(dà)制(zhì)藥巨頭青睐。近年來(lái)其與Genmab(5.5億美元)、Amgen(13 億美元)、 Roche(10億美元)、Celgene(15.9億美元)、GSK(10億美元)、BMS(9.2億美元)等多(duō)家(jiā)合作(zuò)夥伴聯合開(kāi)發過繼細胞療法和(hé)雙特異性抗體(tǐ)。
2022年6月2日,Immatics與BMS共同宣布,雙方擴大(dà)戰略聯盟以開(kāi)發多(duō)種同種異體(tǐ)現貨型TCR-T和(hé)/或CAR-T項目。本次合作(zuò)總額超14億美元。同月7日,Immatics又與CRISPR基因編輯技(jì)術(shù)奠基人(rén)之一張鋒創立的Editas Medicine共同宣布,兩家(jiā)公司已達成戰略研究合作(zuò)和(hé)許可(kě)協議,将γδT 細胞過繼細胞療法和(hé)基因編輯相結合,以開(kāi)發用于治療癌症的藥物。
核心技(jì)術(shù):基于 CRISPR 基因編輯的 NK 細胞療法
2022動向:與賽諾菲達成10.25億美元
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://www.scribetx.com/
Scribe總部位于美國加利福尼亞州,由CRISPR發明(míng)者以及領先的分子工程師(shī)Jennifer Doudna、Benjamin Oakes、Brett Staahl、David Savage共同創立,專注于為(wèi)基于CRISPR的基因醫(yī)學設計(jì)最先進平台。公司已累計(jì)完成1.2億美元融資。
CRISPR是細菌和(hé)病毒進行(xíng)鬥争産生(shēng)的免疫武器(qì),可(kě)以在細菌中進化為(wèi)“基因破壞”形式,以抵禦病原體(tǐ)。它在細菌中非常有(yǒu)效,但(dàn)當研究人(rén)員試圖将其用于人(rén)類時(shí)會(huì)遇到各種障礙。例如,對于體(tǐ)內(nèi)編輯,Cas9的大(dà)小(xiǎo)使其不适合用于體(tǐ)內(nèi)基因編輯療法遞送的腺相關病毒(AAV)。
Scribe的X-editing (XE)技(jì)術(shù)是一項以創新CasX酶為(wèi)基礎的系統。2019年,Jennifer Doudna團隊在Nature上(shàng)發表論文,證實了其于2016年發現的新型Cas蛋白——CasX可(kě)以用于基因組編輯,并揭示了新型基因組編輯工具CRISPR/CasX的潛在機制(zhì),該工具使用獨特的結構進行(xíng)可(kě)編程的雙鏈DNA結合和(hé)切割。CasX最重要的應用特點在于其比Cas9、Cas12a都要小(xiǎo)得(de)多(duō),隻有(yǒu)不到1000個(gè)氨基酸,可(kě)被包裹在AAV載體(tǐ)中。CasX不僅小(xiǎo)巧,還(hái)具有(yǒu)獨特的可(kě)編程編輯方式,具備先前CRISPR-Cas基因組編輯技(jì)術(shù)缺乏的優勢。
Scribe目前共有(yǒu)5個(gè)研發方向,包括:
神經系統疾病(亨廷頓舞蹈症、家(jiā)族性漸凍症、脊髓性肌萎縮症、帕金森(sēn)病、早發性家(jiā)族性阿爾茨海默症、天使綜合征等);
眼科疾病(色素性視(shì)網膜炎、視(shì)錐-視(shì)杆細胞營養不良、先天性黑(hēi)蒙症、青光眼、全色盲等);
多(duō)系統、肌肉和(hé)代謝疾病(囊性纖維化、杜氏肌營養不良、α1-抗胰蛋白酶缺乏症、早衰症、家(jiā)族性高(gāo)膽固醇血症、苯丙酮尿症等);
造血功能障礙疾病(鐮狀細胞病、重度聯合免疫缺陷、範可(kě)尼貧血、血友(yǒu)病A/B、慢性肉芽腫、血管性血友(yǒu)病);
細胞療法(CAR-T、NK、TiL、HSC、iPSC)。
 來(lái)源:Scribe Therapeutics官網
來(lái)源:Scribe Therapeutics官網
近年來(lái),Scribe已先後與制(zhì)藥巨頭渤健、賽諾菲達成戰略合作(zuò)。2022年9月27日,賽諾菲宣布與 Scribe達成超10億美元的合作(zuò),開(kāi)發基于 CRISPR 基因編輯的 NK 細胞療法來(lái)對抗癌症。在此之前(2020年10月),Scribe 曾與渤健達成超4億美元合作(zuò),共同開(kāi)發基于CRISPR的療法,以解決導緻肌萎縮性側索硬化症(ALS)的潛在遺傳病因。
核心技(jì)術(shù): 通(tōng)用型CAR-NK細胞療法
2022動向:增發2.3億美元+公布了兩款CAR-NK在研産品的積極初步臨床數(shù)據
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://www.nkartatx.com/
Nkarta Therapeutics成立于2015年,是一家(jiā)專注于開(kāi)發同種異體(tǐ)現貨型NK細胞療法用于癌症治療的臨床階段生(shēng)物制(zhì)藥公司。2020年7月10日,Nkarta登陸納斯達克拟募集資金2.52億美元。上(shàng)市前,該公司累計(jì)完成了1.25億美元融資。
Nkarta公司專有(yǒu)的NK細胞治療平台旨在通(tōng)過增強靶向性、大(dà)量的擴增和(hé)延長這些(xiē)免疫細胞的持久性,最大(dà)限度地提高(gāo)NK細胞的治療效果,從而釋放出強大(dà)而持久的抗癌免疫介導攻擊。
為(wèi)了提高(gāo)NK細胞的抗腫瘤活性,一般會(huì)系統輸注臨床級的重組IL2或者單鏈IL15細胞因子,然而,這種方法往往伴随嚴重的不良反應,且IL2輸注往往同時(shí)導緻抑制(zhì)性免疫細胞Treg的擴增,抑制(zhì)NK細胞的活性。因此,NK細胞臨床試驗多(duō)使用IL15。Nkarta公司通(tōng)過基因工程的方法,使外周血NK細胞表達膜結合的IL15(mbIL15),提高(gāo)了NK細胞的存活、增殖、殺傷能力。
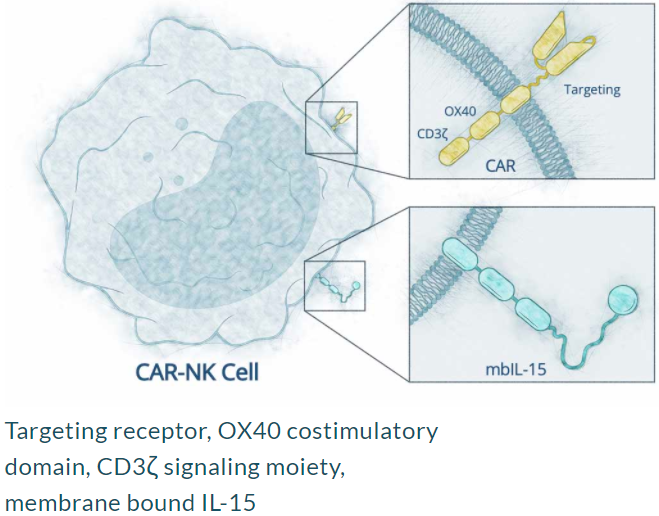 Nkarta公司設計(jì)的CAR-NK(來(lái)源:Nkarta官網)
Nkarta公司設計(jì)的CAR-NK(來(lái)源:Nkarta官網)
2022年4月,Nkarta公布了兩款CAR-NK在研産品:靶向NKG2D的NKX101和(hé)靶向CD19的NKX019治療血液瘤的積極初步臨床數(shù)據。NKX019治療複發/難治性非霍奇金淋巴瘤(r/r NHL) 患者,高(gāo)劑量組6例中5例(83%)獲得(de)了緩解(ORR),其中3例(50%)獲得(de)了完全緩解(CR)。受此消息影(yǐng)響,該公司股價上(shàng)漲140%。2022年12月,該公司又公布NKX019作(zuò)為(wèi)單藥治療 r/r NHL 患者的I期 積極研究結果,較高(gāo)劑量水(shuǐ)平治療組CR達70%,再振人(rén)心。
2022年4月28日,Nkarta宣布完成增發的2.3億美元融資,并拟将這筆收益用于資助 NKX101和(hé) NKX019的臨床開(kāi)發、研究階段項目的臨床前研究以及內(nèi)部制(zhì)造能力的持續建設。
核心技(jì)術(shù):邏輯門(mén)控CAR-T
2022動向:B輪融資2.2億美元+與BMS、羅氏建立合作(zuò)
魔方評分:⭐⭐⭐⭐
公司官網:https://www.arsenalbio.com/
Arsenal Biosciences成立于2019年,專注于整合基于CRISPR的基因編輯、規模化高(gāo)通(tōng)量靶點識别、合成生(shēng)物學和(hé)機器(qì)學習等技(jì)術(shù),以推進免疫細胞療法的發現和(hé)開(kāi)發新範式。該公司正在構建行(xíng)業中最大(dà)型的治療增強整合回路文庫,利用邏輯門(mén)控改善腫瘤靶向,并且通(tōng)過合成生(shēng)物學讓CAR-T療法具有(yǒu)行(xíng)使多(duō)種藥物功能的潛力。
2022年9月,Arsenal完成2.2億美元B輪融資,目前累計(jì)融資金額超3億美元。此外,2022年其與跨國制(zhì)藥巨頭也達成了兩項合作(zuò):1月,Arsenal宣布擴大(dà)與BMS的戰略合作(zuò),以發現和(hé)推進用于治療實體(tǐ)瘤的T細胞療法;9月,Arsenal與羅氏旗下基因泰克達成7000萬美元合作(zuò)協議, 運用Arsenal專有(yǒu)科技(jì)進行(xíng)高(gāo)通(tōng)量篩選與T細胞工程化,以識别T細胞類療法成功的關鍵樞紐,開(kāi)發未來(lái)實體(tǐ)瘤療法。
公司聯合創始人(rén)之一,加州大(dà)學舊(jiù)金山(shān)分校(xiào)的Kole Roybal教授,憑借其開(kāi)發的全新T細胞免疫療法成為(wèi)2018年首屆Sartorius & Science Prize for Regenerative Medicine & Cell Therapy大(dà)獎得(de)主。2021年其在Science Translational Medicine發表的幾篇論文指出,名為(wèi)synNotch的調控系統能夠提高(gāo)CAR-T細胞靶向特異性,提高(gāo)細胞療法的持久性。
 Kole Roybal教授(來(lái)源:Arsenal官網)
Kole Roybal教授(來(lái)源:Arsenal官網)
值得(de)一提的是,Arsenal也上(shàng)榜了由生(shēng)物醫(yī)藥行(xíng)業知名媒體(tǐ)網站(zhàn)BioSpace評選的2021年度新一代(NextGen)生(shēng)物新銳公司。入選公司皆在近幾年成立,BioSpace通(tōng)過對公司資本助力、合作(zuò)、研發管線、成長潛力以及創新方面進行(xíng)綜合評估。Arsenal的入選也體(tǐ)現其短(duǎn)短(duǎn)幾年內(nèi)對業界産生(shēng)了重大(dà)影(yǐng)響。
核心技(jì)術(shù):基于合成生(shēng)物學開(kāi)關技(jì)術(shù)的TCR-T
2022動向:1.75億美元的A輪融資 + 與Metagenomi建立合作(zuò) + 入圍“Most Promising Biotech Startups of 2022”榜單
魔方評分:⭐⭐⭐⭐
公司官網:https://www.affinittx.com/
Affini-T Therapeutics是一家(jiā)專注于T細胞免疫療法的初創公司,成立于2021年,總部位于波士頓。公司緻力于通(tōng)過調節免疫系統來(lái)靶向緻癌驅動突變,為(wèi)難治性實體(tǐ)瘤患者開(kāi)發可(kě)能改善生(shēng)活的藥物。公司創始團隊及科學顧問委員會(huì)陣容豪華,包括Fred Hutchinson癌症研究中心免疫學負責人(rén)、癌症免疫治療專家(jiā)Phil Greenberg博士,癌症免疫療法先驅、諾貝爾生(shēng)理(lǐ)學或醫(yī)學獎得(de)主Jim Allison教授,知名癌症免疫療法轉化科學家(jiā)Pam Sharma教授等。
Affini-T的基礎細胞療法平台建立在創始團隊開(kāi)創性工作(zuò)的基礎上(shàng),旨在利用T細胞受體(tǐ)(TCR)發現引擎和(hé)一套合成生(shēng)物學組件,開(kāi)發靶向KRAS和(hé)p53等緻癌驅動突變的潛在best-in-class療法。
具體(tǐ)來(lái)說,該公司團隊利用先進的合成生(shēng)物學和(hé)基因編輯技(jì)術(shù),開(kāi)創性地設計(jì)TCR-T細胞療法以靶向緻癌驅動突變。公司的TCR發現平台是一個(gè)強大(dà)的引擎,可(kě)用于識别罕見的高(gāo)親和(hé)力TCR,在實體(tǐ)瘤中釋放免疫應答(dá)。此外,Affini-T利用專有(yǒu)的合成生(shēng)物學開(kāi)關受體(tǐ)來(lái)重編程免疫細胞,可(kě)顯著改善T細胞在敵對腫瘤微環境中的增殖存活以及持久反應的能力。
 Affini-T的技(jì)術(shù)通(tōng)過協調CD4/CD8的協同反應,引發更深入和(hé)顯著的抗腫瘤效應。(來(lái)源:Affini-T官網)
Affini-T的技(jì)術(shù)通(tōng)過協調CD4/CD8的協同反應,引發更深入和(hé)顯著的抗腫瘤效應。(來(lái)源:Affini-T官網)
核心技(jì)術(shù): 基于基因回路技(jì)術(shù)的同種異體(tǐ)CAR-NK
2022動向:與 DYNS 合并業務并上(shàng)市,預計(jì)總收益約為(wèi) 1.565 億美元
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://www.sentibio.com/
Senti Biosciences是一家(jiā)利用利用合成生(shēng)物學設計(jì)“基因回路”以改善細胞和(hé)基因治療産品 的初創公司,出道(dào)即自帶 “光環”,由合成生(shēng)物學奠基人(rén)James J. Collins及其學生(shēng)盧冠達等于2016年聯合創辦。公司使命是用更智能的藥物來(lái)戰勝複雜的疾病,從而改變人(rén)們的生(shēng)活。在宣布合并上(shàng)市前,Senti Bio累計(jì)完成了約2億美元的融資。
Senti Bio的基因回路是一種新穎的、專有(yǒu)的DNA組合,使細胞能夠感知環境、執行(xíng)邏輯并指導細胞産生(shēng)治療性蛋白質,從而提高(gāo)安全性和(hé)療效。該公司相信,其在活細胞中編程基因回路的方法可(kě)以使藥物開(kāi)發者在幾乎任何細胞或基因藥物中構建最佳功能。公司專有(yǒu)平台包括特定的基因回路技(jì)術(shù),如邏輯門(mén)、小(xiǎo)分子調節器(qì)、組合有(yǒu)效載荷和(hé)合成啓動子,這些(xiē)技(jì)術(shù)有(yǒu)可(kě)能賦予細胞和(hé)基因治療産品更高(gāo)的療效、精确度和(hé)控制(zhì)能力。
Senti Bio的腫瘤學管線主要專注于3個(gè)臨床前階段項目:SENTI-202,一種邏輯門(mén)控(OR+NOT)現貨型CAR-NK細胞療法,旨在靶向和(hé)消除急性髓系白血病(AML)細胞,同時(shí)避免損傷健康骨髓;SENTI-301,一種可(kě)調節的多(duō)臂現貨型CAR-NK細胞療法,用于治療肝細胞癌(HCC);SENTI-401,一種邏輯門(mén)控(NOT)現貨型CAR-NK細胞療法,旨在靶向和(hé)消除結直腸癌(CRC)細胞,同時(shí)避免損傷其他部位的健康細胞。此外,該公司還(hái)與羅氏子公司Spark Therapeutics 和(hé)拜耳子公司 BlueRock Therapeutics合作(zuò),将其基因回路技(jì)術(shù)應用于腫瘤學以外的領域。
2021年 12 月底,Senti Bio宣布與 DYNS 的SPAC 合并協議,預計(jì)合并總收益預計(jì)将超 2.96 億美元。當時(shí)公告指出,雙方的合并交易已獲得(de) DYNS 和(hé) Senti Bio 董事會(huì)的批準,預計(jì)合并的時(shí)間(jiān)為(wèi) 2022 年第二季度。2022年6月,Senti Bio與SPAC 合并上(shàng)市交易如期完成,預計(jì)總收益約為(wèi) 1.565 億美元 。
核心技(jì)術(shù):靶向實體(tǐ)瘤CAR-T
2022動向:B輪融資超1.2億美元
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://www.oricell.com/
原啓生(shēng)物成立于2015年,在2019年底獲得(de)啓明(míng)創投近億元的Pre-A輪獨家(jiā)投資後,作(zuò)為(wèi)生(shēng)物創新藥研發資産從原能細胞集團剝離,開(kāi)始以創新型細胞治療技(jì)術(shù)平台為(wèi)核心,聚焦于腫瘤免疫治療領域的産品開(kāi)發。
2022年3月, 原啓生(shēng)物宣布任命原複星凱特CTO崔衛東博士為(wèi)首席技(jì)術(shù)官,負責公司工藝開(kāi)發及生(shēng)産,加速推動公司靶向實體(tǐ)瘤的CAR-T産品臨床注冊及未來(lái)商業化進展。8月,原啓生(shēng)物宣布完成總金額超過1.2億美元的B輪融資,資金将主要用于推進公司十餘條經過充分概念驗證(POC)的腫瘤細胞治療産品管線的開(kāi)發和(hé)商業化進程,繼續完善公司自主創新技(jì)術(shù)平台的建設,以及未來(lái)商業化生(shēng)産基地的規劃與建設。
 原啓生(shēng)物CAR-T産品管線(來(lái)源:原啓生(shēng)物官網)
原啓生(shēng)物CAR-T産品管線(來(lái)源:原啓生(shēng)物官網)
在産品研發進展方面,公司首個(gè)自主開(kāi)發靶向GPC3治療晚期肝癌的CAR-T産品(Ori-C101)的臨床試驗申請(qǐng)(IND)獲得(de)了國家(jiā)食品藥品監督管理(lǐ)局藥品審評中心(CDE)的受理(lǐ)。在過往的臨床研究中,Ori-C101已經在GPC3陽性晚期肝癌患者中表現出良好安全性和(hé)有(yǒu)效性。
原啓生(shēng)物開(kāi)發的中國首款GPRC5D CAR-T産品OriCAR-017 用于治療r/r MM,其研究者發起的I期臨床試驗(POLARIS)充分證實了該産品極大(dà)的開(kāi)發前景。原啓生(shēng)物以口頭報告形式分别在2022 ASCO、2022 EHA年會(huì)上(shàng)公布了截止至2022年4月30日的臨床結果。數(shù)據顯示,包括5例既往BCMA CAR-T治療失敗的受試者在內(nèi)的所有(yǒu)受試者,均獲得(de)100%客觀緩解率(ORR)和(hé)100%微小(xiǎo)殘留病竈(MRD)陰性率,持續無進展,無需任何額外抗腫瘤治療以及良好的安全性。目前,原啓生(shēng)物正加快推進其中美兩地的注冊及臨床開(kāi)發速度。
核心技(jì)術(shù):下一代自體(tǐ)和(hé)同種異體(tǐ)CAR-T
2022動向:與羅氏達成超60億美元的合作(zuò)+ 增發8050萬美元
魔方評分:⭐⭐⭐⭐⭐
公司官網:https://poseida.com/

2023年第41屆摩根大(dà)通(tōng)醫(yī)療保健會(huì)議(JPM)正式恢複線下召開(kāi)。
在第一天的報告出現了不少(shǎo)細胞與基因治療的公司,有(yǒu)不少(shǎo)公司都帶來(lái)了自己對2023年的積極展望,例如手握潛在首款DMD基因療法的Serepta公司、首款治療血友(yǒu)病A的獲批基因療法的BioMarin等;也有(yǒu)目前在監管問題中掙紮的一些(xiē)公司:例如遭FDA臨床暫停的Beam、裁員換血的Editas等。
bioSeedin将聚焦于Day 1 中的細胞與基因療法部分,對其公開(kāi)的報告進行(xíng)整理(lǐ)與綜合。
在周一上(shàng)午的演講中,諾華首席執行(xíng)官Vas Narasimhan表示:公司的 2023 年戰略側重于五個(gè)治療領域:心血管、免疫學、神經科學、實體(tǐ)瘤和(hé)血液學。
Narasimhan說,該公司計(jì)劃在這些(xiē)領域取得(de)進展的方式之一是通(tōng)過其基因治療産品組合,并且表示諾華“內(nèi)部有(yǒu)超過15個(gè)項目正在繼續推進”。
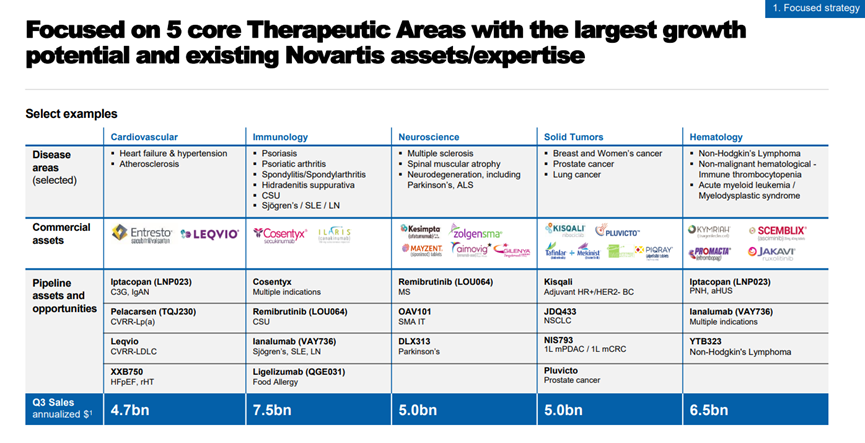
在免疫學方面,Narasimhan表示,諾華将使用其T-Charge平台将把大(dà)部分精力集中在細胞和(hé)基因治療上(shàng)。
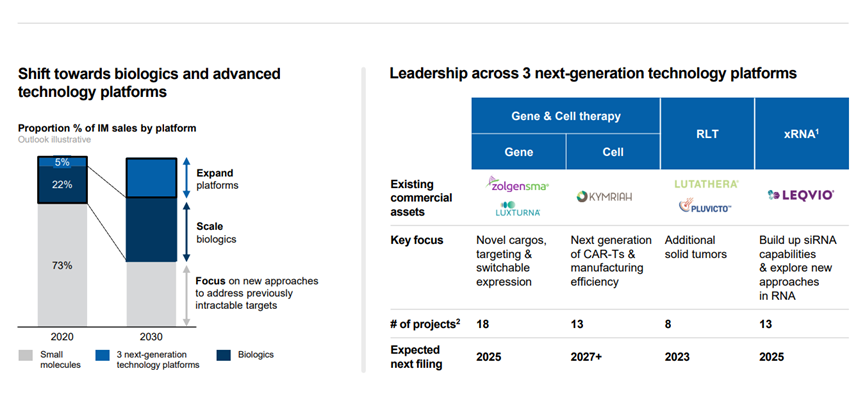
此外,諾華還(hái)特别指出了近期即将要公布臨床試驗讀數(shù)的關鍵資産。

中午 12:12,Prime Medicine首席執行(xíng)官Keith Gottesdiener在JPM23會(huì)議上(shàng)發表演講。Prime Medicine是劉如謙參與創立的第3家(jiā)上(shàng)市公司,專注于使用Prime Editing 技(jì)術(shù)進行(xíng)基因編輯。

Keith提到近期基因療法在FDA的屢屢碰壁,表示這些(xiē)都是“成長的痛苦”,可(kě)能會(huì)在未來(lái)幾年內(nèi)得(de)到解決。與此同時(shí),他表示Prime公司擁有(yǒu)“強大(dà)的現金跑道(dào)”,暫時(shí)不擔心資金問題。
Prime 有(yǒu) 18 個(gè)項目正在開(kāi)發中,不過都處于非常早期的階段。
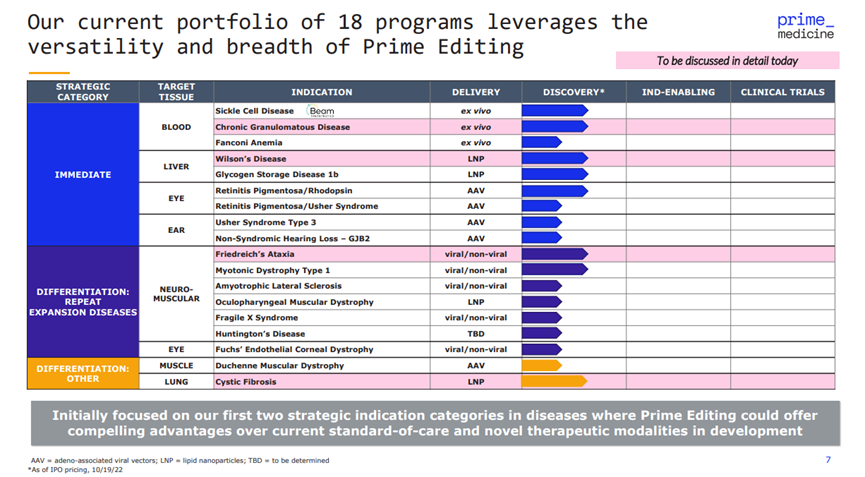
Keith表示,2023年,公司将着重尋找BD交易與外部合作(zuò)的機會(huì)。
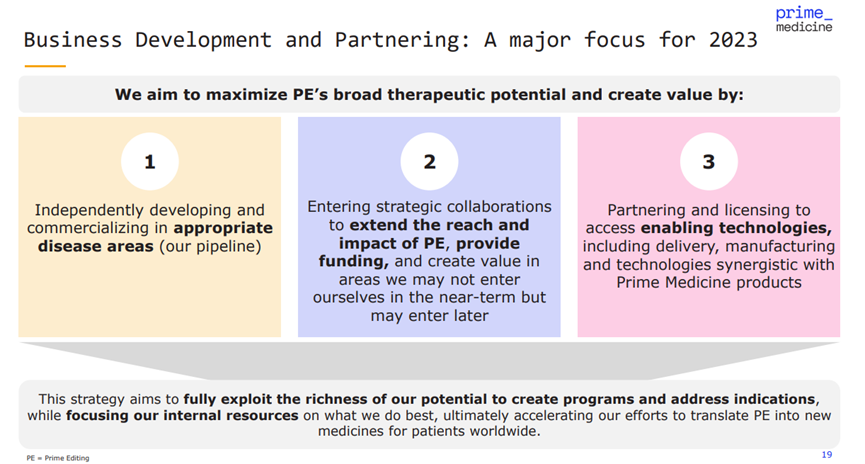
下午 12:51,BioMarin董事長兼首席執行(xíng)官J.J. Bienaimé發表演講,稱其基因治療産品Roctavian為(wèi)迄今為(wèi)止“最強勁的産品”。

Roctavian是一款治療嚴重血友(yǒu)病A的基因療法,使用AAV5病毒載體(tǐ)遞送表達凝血因子VIII的轉基因。今年8月24日,歐盟委員會(huì)(EC)批準此基因療法有(yǒu)條件上(shàng)市,成為(wèi)首款用于治療血友(yǒu)病A的基因療法。
近日,BioMarin公司宣布了Roctavian取得(de)3期臨床的積極結果,該試驗的随訪時(shí)間(jiān)超過了3年。這是目前規模最大(dà),持續時(shí)間(jiān)最長的血友(yǒu)病基因療法全球3期臨床試驗。

試驗結果顯示,在治療3年和(hé)4年的患者中,其凝血因子VIII的活性平均值分别為(wèi)18.8和(hé)15.2,中位數(shù)值為(wèi)8.4和(hé)7.4。兩組的平均年出血事件率分别為(wèi)1.0和(hé)0.8,而中位值都為(wèi)0.0。此外,兩組的年凝血因子平均使用次數(shù)分别為(wèi)8.4和(hé)11.1,中位值也均為(wèi)0。與基線值相比,在治療的第三年後,患者的平均年出血事件率減少(shǎo)了80%,而凝血因子VIII的使用減少(shǎo)了94%。
Bienaimé表示,他預計(jì)超過75%的美國處方者将在上(shàng)市後一年內(nèi)采用Roctavian來(lái)治療嚴重的成人(rén)血友(yǒu)病A患者。加上(shàng)Voxzogo,一種用于增加軟骨發育不全兒童(5歲及以上(shàng))線性生(shēng)長的療法,Bienaimé預測到十年中期BioMarin的增長将達到40億至50億美元。
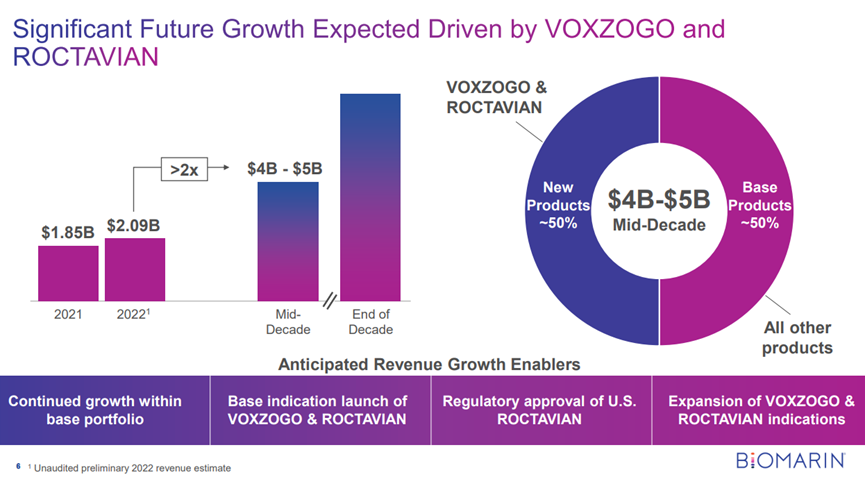
下午 1:30,Sarepta Therapeutics總裁兼首席執行(xíng)官Doug Ingram發表報告。

11月,FDA接受了Sarepta 公司的BLA申請(qǐng),如果獲得(de)批準,SRP-9001将成為(wèi)市場(chǎng)上(shàng)第一個(gè)針對杜氏肌營養不良(DMD)的基因療法。FDA已将PDUFA日期定為(wèi)2023年5月29日。
SRP-9001是通(tōng)過AAV将編碼微肌營養不良蛋白的基因傳遞到肌肉組織,使肌肉細胞表達對應的蛋白,從而減緩或阻止肌肉退化。
該療法采用從非人(rén)靈長類動物中分離出的AAVrh74病毒載體(tǐ),此病毒載體(tǐ)優點是能夠在肌肉中引起轉基因的強力表達,不會(huì)穿過血腦(nǎo)屏障進入中樞神經系統,且較少(shǎo)患者體(tǐ)內(nèi)存在針對這一病毒載體(tǐ)的中和(hé)抗體(tǐ)。
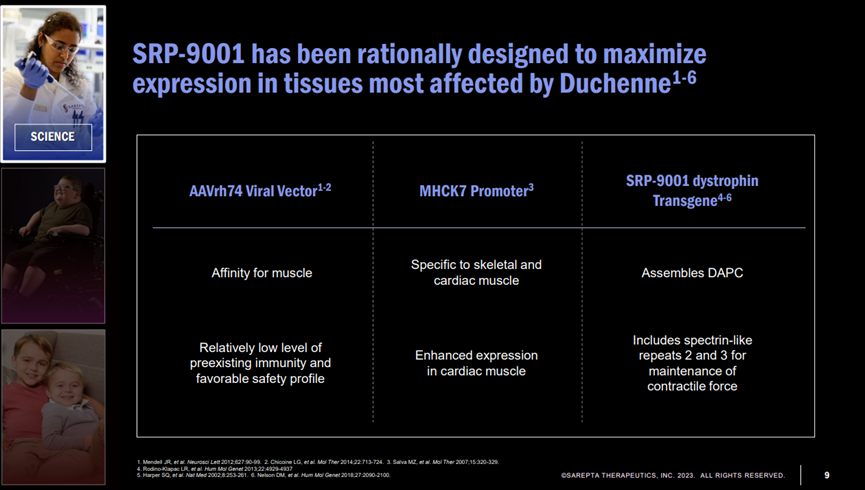
Doug Ingram在大(dà)會(huì)上(shàng)公布了相關數(shù)據,其中包括臨床前動物模型,功能數(shù)據和(hé)生(shēng)物标志(zhì)物等,大(dà)量臨床前和(hé)臨床數(shù)據支持SRP-9001的療效。

下午4:47,Beam Therapeutics公司發表演講,該公司密切關注關注鐮狀細胞療法的市場(chǎng)。

Beam 公司報告了公司血液學,免疫腫瘤學和(hé)遺傳疾病産品組合的進展,并提供了預期即将到來(lái)的裏程碑的最新情況。

第三季度财報中,Beam Therapeutics表示将停止對BEAM-102的IND申請(qǐng)進程。BEAM-102用于治療鐮狀細胞病,通(tōng)過直接編輯導緻病變的血紅蛋白S點突變來(lái)重建正常的人(rén)類血紅蛋白。
今年7月,FDA暫停了其CAR-T 療法BEAM-201的IND申請(qǐng),後又得(de)到解除。BEAM-201針對CD7靶點,是首個(gè)同時(shí)針對4個(gè)基因展開(kāi)編輯的CAR-T療法。
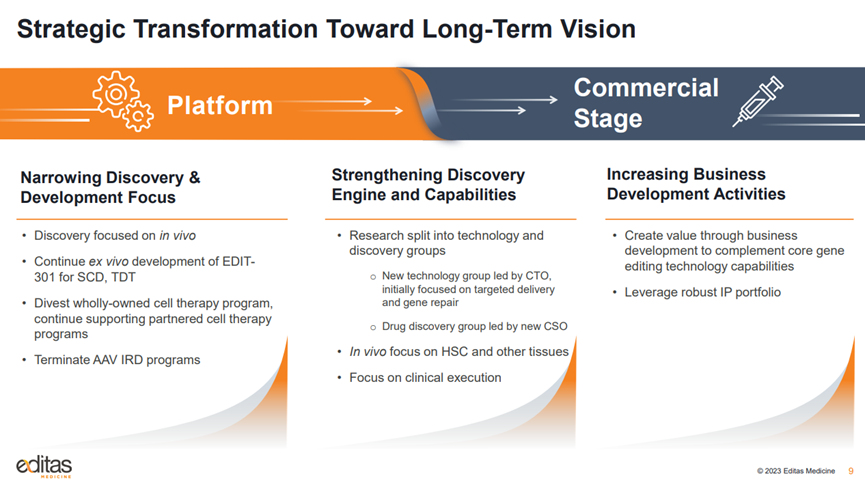
下基因編輯公司Editas Medicine在JPM宣布了重要戰略更新,包括投資組合重新确定優先級和(hé)研發調整。該公司由張鋒、劉如謙共同創立,于2016年上(shàng)市,是全球CRISPR基因編輯領域首家(jiā)IPO的公司。

Editas表示,将停止對遺傳性視(shì)網膜疾病和(hé)臨床前全資擁有(yǒu)的iNK項目的內(nèi)部投資,專注于血紅蛋白病和(hé)體(tǐ)內(nèi)基因編輯。公司将資源優先分配給EDIT-301,該項目用于治療嚴重鐮狀細胞病和(hé)輸血依賴性β地中海貧血。
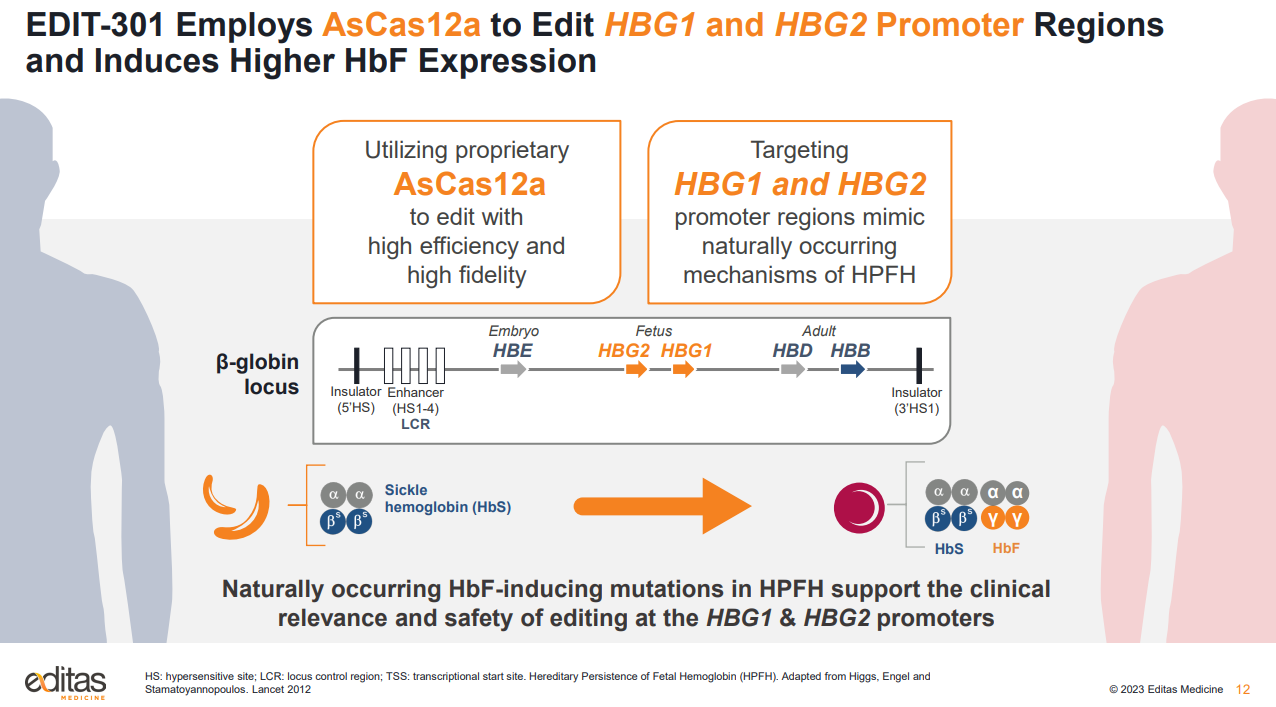
Editas希望為(wèi)遺傳性眼病項目EDIT-101和(hé)EDIT-103尋找外部合作(zuò)夥伴,但(dàn)會(huì)繼續開(kāi)發合作(zuò)研發的細胞療法項目。
Editas裁員了20%,預計(jì)将把公司的現金跑道(dào)延長到2025年。此外,首席科學官Mark S. Shearman博士将從2023年3月31日起離開(kāi)公司。