
此前,在美國第61屆血液學會(huì)年會(huì)上(shàng),研究人(rén)員報道(dào)一種新型異體(tǐ)CD83嵌合抗原受體(tǐ)(CD83 CAR-T)。體(tǐ)內(nèi)異種移植物抗宿主病(GVHD)模型評估結果顯示,與模拟轉導T細胞組的小(xiǎo)鼠相比,注射CD83 CAR-T的小(xiǎo)鼠可(kě)以顯着提高(gāo)存活率,注射第21天GVHD靶器(qì)官損傷幾乎可(kě)以忽略,CD1c+、CD83+樹(shù)突狀細胞、CD4+、CD83+ T細胞和(hé)緻病性Th1細胞在第21天時(shí)顯著減少(shǎo),Treg與同種異體(tǐ)Tconv的比值也顯著增加,且顯示出很(hěn)好的耐受性。此外,研究表明(míng)CD83 CAR-T能有(yǒu)效殺死急性髓系白血病(AML)細胞系,靶點和(hé)腫瘤外的毒性可(kě)忽略不計(jì)。CD83 CAR-T細胞可(kě)以作(zuò)為(wèi)一種新的異體(tǐ)CAR-T療法對髓系惡性腫瘤發揮殺傷的同時(shí)也能很(hěn)好地避免GVHD的發生(shēng)。
CAR-T療法改變了血液惡性腫瘤治療前景,目前雖已有(yǒu)兩款針對血液惡性腫瘤的自體(tǐ)型CAR-T上(shàng)市,但(dàn)仍有(yǒu)一些(xiē)瓶頸限制(zhì)其發展。首先,目前自體(tǐ)型CAR-T的T細胞來(lái)源于患者自身,屬于自身訂制(zhì)産品,且生(shēng)産工藝複雜,周期較長,晚期病人(rén)在CAR-T細胞生(shēng)産過程中病情不斷惡化,可(kě)能錯過最佳治療時(shí)間(jiān),這在某些(xiē)高(gāo)度增殖性疾病(如急性白血病)患者中尤其成問題。其次,很(hěn)多(duō)接受多(duō)次化療的病人(rén)很(hěn)難獲得(de)足量且健康的T細胞,這限制(zhì)了CAR-T細胞的制(zhì)備。最後,每個(gè)患者的T細胞都有(yǒu)差異,無法保證産品的穩定和(hé)質量控制(zhì),很(hěn)難生(shēng)産出标準化的産品。
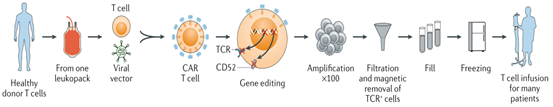 圖1 自體(tǐ)CAR-T的生(shēng)産工藝
圖1 自體(tǐ)CAR-T的生(shēng)産工藝與自體(tǐ)方法相比,使用利用健康捐贈者的細胞生(shēng)産的異體(tǐ)CAR-T有(yǒu)許多(duō)潛在的優勢,如易于規模化和(hé)批量生(shēng)産從而降低(dī)了成本。大(dà)量的CAR-T細胞可(kě)以由單個(gè)供體(tǐ)生(shēng)産,可(kě)以立即用于不同患者治療,簡化治療流程。
然而,異體(tǐ)CAR-T也有(yǒu)兩個(gè)常見的問題。首先,給藥的同種異體(tǐ)T細胞可(kě)能導緻移植物抗宿主病(GVHD)。其次,這些(xiē)異體(tǐ)CAR-T細胞可(kě)能被宿主免疫系統迅速清除,限制(zhì)其抗腫瘤活性。下文介紹不同來(lái)源的異體(tǐ)CAR-T療法,以及優化當前異體(tǐ)CAR -T細胞的方法。
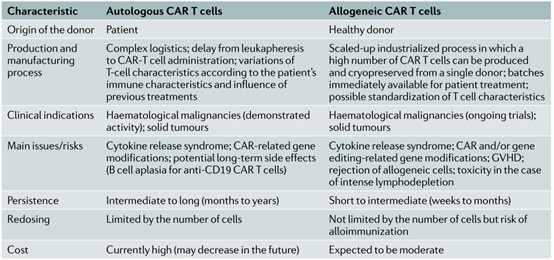 表1 自體(tǐ)CAR-T與異體(tǐ)CAR-T
表1 自體(tǐ)CAR-T與異體(tǐ)CAR-T
目前用于制(zhì)造異體(tǐ)CAR-T的T細胞主要來(lái)源于外周血單個(gè)核細胞(PBMCs),少(shǎo)部分來(lái)源于臍帶血(UCB)。原則上(shàng),這些(xiē)T細胞也可(kě)以從再生(shēng)幹細胞中獲得(de),如誘導多(duō)能幹細胞(iPSCs)或胚胎幹細胞。因為(wèi)異體(tǐ)CAR-T細胞是由健康的供體(tǐ)産生(shēng)的,與自體(tǐ)CAR-T細胞相比,這些(xiē)細胞沒有(yǒu)受到病人(rén)腫瘤的免疫效應或化療藥物的影(yǐng)響。根據免疫特性選擇供體(tǐ)細胞可(kě)能是減少(shǎo)GVHD異質性的關鍵因素。
使用UCB衍生(shēng)的CAR-T細胞可(kě)降低(dī)GVHD的發病率和(hé)嚴重程度。來(lái)源于臍帶血的T細胞具有(yǒu)獨特的抗原初始狀态,這可(kě)能是臍帶血移植物的同種反應性降低(dī)的原因。胎盤來(lái)源的幹細胞可(kě)以用來(lái)産生(shēng)T細胞或自然殺傷(NK)細胞。胎盤具有(yǒu)獨特的HLA表達模式,與其它組織不同,絨毛外細胞滋養層細胞隻表達HLA-C、HLA-E和(hé)HLA-G,合胞滋養層細胞HLA陰性。這些(xiē)特異性對胎盤來(lái)源的T細胞的影(yǐng)響暫時(shí)還(hái)沒有(yǒu)相關研究報道(dào)。
iPSCs的T細胞也可(kě)以作(zuò)為(wèi)異體(tǐ)CAR-T細胞的來(lái)源。理(lǐ)論上(shàng)講,iPSCs細胞系具有(yǒu)無限的自我更新能力,可(kě)以無限期地儲存和(hé)使用。可(kě)以用具有(yǒu)共同HLA單倍型的iPSCs以最小(xiǎo)化iPSCs CAR-T細胞的免疫排斥反應風險。使用iPSCs的另外一個(gè)優點是CAR-T細胞是由一個(gè)克隆多(duō)能幹細胞系産生(shēng)的,因此是均勻的。
供體(tǐ)和(hé)受體(tǐ)之間(jiān)的HLA不匹配觸發免疫識别,可(kě)能導緻移植物排斥反應及GVHD。GVHD是SCT發病和(hé)死亡的主要原因,研究表明(míng)αβ 型T細胞在急慢性GVHD發病中起着重要作(zuò)用。αβ型T細胞的TCR識别主要組織相容性複合物(MHC)分子(人(rén)類的HLA系統)位點。而MHC位點是人(rén)類基因組中最具多(duō)态性的區(qū)域,導緻了成千上(shàng)萬的MHC差異表達。αβ 型T細胞與外源MHC分子相互作(zuò)用,是移植排斥反應和(hé)GVHD的關鍵。目前,有(yǒu)幾種策略降低(dī)異體(tǐ)CAR-T療法發生(shēng)GVHD的風險。
這種方法僅限于接受同種異體(tǐ)幹細胞移植(SCT)但(dàn)随後複發的患者,在這種情況下,CAR-T細胞可(kě)以從原始供體(tǐ)中獲得(de)。在最近的一份報告中,20例B細胞惡性腫瘤患者輸注來(lái)自同一供體(tǐ)的CD19 CAR-T細胞後,6例完全緩解,2例部分緩解,且無GVHD産生(shēng)。緩解期患者血CAR-T細胞水(shuǐ)平高(gāo)于未緩解期患者,3周後CAR-T細胞顯著下降。該結果顯示異體(tǐ)來(lái)源的CAR-T細胞可(kě)能被納入同種異體(tǐ)SCT的策略中,以增強移植物抗腫瘤效應,而不會(huì)增加GVHD的風險。
NK細胞最初被鑒定為(wèi)具有(yǒu)殺死腫瘤細胞的能力,是機體(tǐ)天然腫瘤免疫監視(shì)的一個(gè)組成部分。NK細胞對細胞具有(yǒu)高(gāo)度的腫瘤細胞溶解性,一些(xiē)研究表明(míng),不同類型的腫瘤中存在NK細胞功能障礙,說明(míng)腫瘤已經進化出逃避NK細胞殺傷的機制(zhì)。因此,通(tōng)過給NK細胞裝備CAR來(lái)增強其抗腫瘤活性是一個(gè)很(hěn)有(yǒu)吸引力的策略。Chu等人(rén)證明(míng)裝備CAR的NK細胞增強了NK細胞的抗腫瘤活性。在另一項研究中,用來(lái)自健康供體(tǐ)的NK細胞表達一種EGFR 靶向CAR,顯示出較好的抗膠質母細胞瘤活性。
外周血中NK細胞濃度相對較低(dī),可(kě)采用體(tǐ)外特異性富集和(hé)擴增NK細胞的策略。表達IL-2 NK92細胞系已被批準用于人(rén)類。使用CD19 CAR–IL–15轉導的NK細胞與CD19 CAR NK細胞對照相比,在異種移植小(xiǎo)鼠淋巴瘤小(xiǎo)鼠模型中具有(yǒu)更長的生(shēng)存期。
γδ型 T細胞能對腫瘤細胞産生(shēng)自然細胞毒性反應,在體(tǐ)外γδ 型T細胞可(kě)以大(dà)量擴增,且不誘發GVHD,因為(wèi)其TCR的激活不受MHC的限制(zhì)。靶向在神經膠質瘤和(hé)其它神經外胚層腫瘤中常過度表達的雙唾液酸神經節苷脂GD2的γδ 型CAR-T增強了對表達GD2腫瘤的殺傷活性。
由于αβ型TCR是産生(shēng)T細胞免疫反應的關鍵因素,研究人(rén)員已經開(kāi)發出阻止TCR在αβ型T細胞表面表達的方法。基因編輯是當今最有(yǒu)前途的方法之一。αβ型T細胞表面的TCR蛋白複合物由α-鏈和(hé)β-鏈組成,β鏈基因包含兩個(gè)恒定區(qū)域,而編碼α鏈的隻有(yǒu)一個(gè)。因此,敲除α鏈編碼基因是破壞αβ型 TCR最直接的方法。Poirot等人(rén)利用TALEN技(jì)術(shù)從健康第三方供體(tǐ)生(shēng)産TCR和(hé)CD52缺陷的CAR-T細胞,在小(xiǎo)鼠模型中沒有(yǒu)産生(shēng)GVHD,并且對 Alemtuzumab有(yǒu)耐藥性,該抗體(tǐ)可(kě)用于消滅宿主表達CD52的T細胞并避免同種排斥反應。
在最新研究中,研究人(rén)員将表達CAR的轉基因直接插入到TRAC基因的位點,在破壞T細胞表達TCR的同時(shí),讓CAR轉基因在TCR基因啓動子調控下表達。動物試驗表明(míng),這種方法産生(shēng)的靶向CD19的CAR-T療法比随機插入CAR基因具有(yǒu)更好的抗腫瘤活性。
目前,多(duō)項在研的異體(tǐ)CAR-T療法已經進入臨床試驗階段,用于治療急性淋巴細胞白血病和(hé)急性髓系白血病患者。
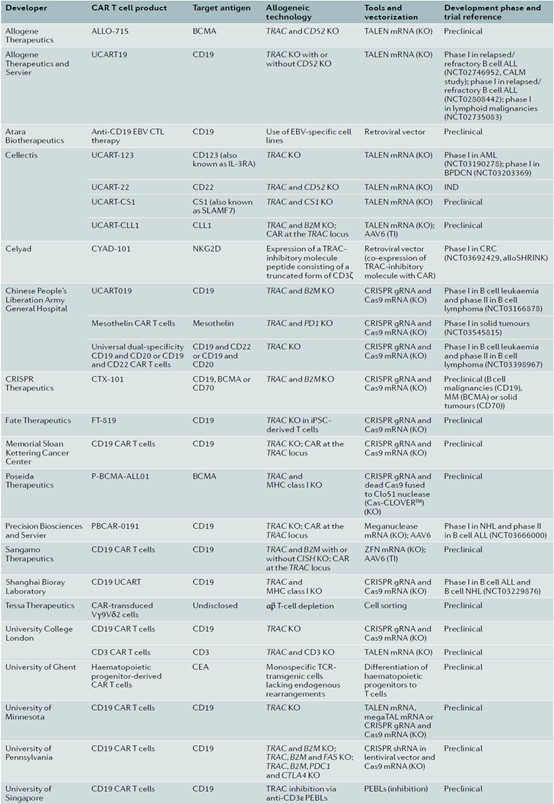
CAR-T細胞治療已經改變了一些(xiē)血液惡性腫瘤的治療前景,目前仍然是最有(yǒu)希望的治療癌症的方法之一。開(kāi)發通(tōng)用CAR-T細胞可(kě)即時(shí)用于患者治療,降低(dī)治療費用,顯著增加該療法的應用範圍。基因編輯技(jì)術(shù)可(kě)通(tōng)過控制(zhì)TCR的表達來(lái)有(yǒu)效消除GVHD産生(shēng)的風險。對于某些(xiē)比較敏感的癌症來(lái)說,異體(tǐ)型CAR-T療法在短(duǎn)期內(nèi)就能起到很(hěn)好的效果,因此不必過于擔心免疫系統排斥的問題。而對于實體(tǐ)瘤,我們希望T細胞在腫瘤附近停留盡量久的時(shí)間(jiān),自體(tǐ)型CAR-T療法則會(huì)有(yǒu)更大(dà)的發揮空(kōng)間(jiān)。目前,盡管在CAR-T治療效率方面仍存在許多(duō)挑戰,尤其是在實體(tǐ)腫瘤中。科研工作(zuò)者也在發揮聰明(míng)才智來(lái)解決這些(xiē)瓶頸,這個(gè)新的治療方法可(kě)能會(huì)使癌症治療發生(shēng)革命性的變化。
轉自:生(shēng)物制(zhì)藥小(xiǎo)編